การจัดเรียงอิเล็กตรอน
การจัดเรียงอิเล็กตรอน
หลักในการจัดเรียงอิเล็กตรอนในอะตอม
1. อิเล็กตรอนที่วิ่งอยู่รอบๆ นิวเคลียสนั้น จะอยู่กันเป็นชั้นๆตามระดับพลังงาน ระดับพลังงานที่อยู่ใกล้นิวเคลียสที่สุด ( ชั้น K) จะมีพลังงานต่ำที่สุด และอิเล็กตรอนในระดับพลังงานชั้นถัดออกมาจะมีพลังงานสูงขึ้นๆ ตามลำดับ พลังงานของอิเล็กตรอนของระดับชั้นพลังงาน K < L < M < N < O < P < Q
หรือชั้นที่ 1< 2 < 3 < 4 < 5 < 6 < 7
หรือชั้นที่ 1< 2 < 3 < 4 < 5 < 6 < 7
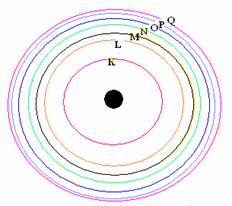
แบบจำลองอะตอมของนีลส์โบร์
2. ในแต่ละชั้นของระดับพลังงาน จะมีจำนวนอิเล็กตรอนได้ ไม่เกิน 2n 2 เมื่อ n = เลขชั้น ซึ่งเลขชั้นของชั้น K=1,L=2,M=3,N=4,O=5,P=6 และ Q=7
ตัวอย่าง จำนวน e - ในระดับพลังงานชั้น K มีได้ ไม่เกิน 2n 2 = 2 x 1 2 = 2x1 = 2
จำนวน e - ในระดับพลังงานชั้น N มีได้ ไม่เกิน 2n 2 = 2 x 4 2 = 2x16 = 32
จำนวน e - ในระดับพลังงานชั้น N มีได้ ไม่เกิน 2n 2 = 2 x 4 2 = 2x16 = 32
ระดับพลังงาน | จำนวนอิเล็กตรอนที่มีได้มากที่สุด |
n = 1 (K) | 2(1) 2 = 2 |
n = 2 (L) | 2(2) 2 = 8 |
n = 3 (M) | 2(3) 2 = 18 |
n = 4 (N) | 2(4) 2 = 32 |
n = 5 (O) | 2(5) 2 = 32 ( 32 คือ เลขมากสุดที่เป็นไปได้ ) |
n = 6 (P) | 2(6) 2 = 32 |
n = 7 (Q) | 2(7) 2 = 32 |
จะเห็นว่ากฎออกเตตมีข้อด้อย คือ เมื่อระดับพลังงานมากกว่า n = 4 จะใช้ไม่ได้ อย่างไรก็ตามในธาตุ 20 ธาตุแรก สามารถใช้การจัดเรียงอิเล็กตรอนตามกฎออกเตตได้ดี
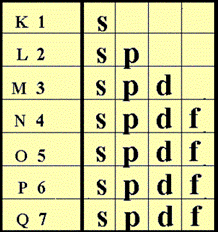
3. ในแต่ละระดับชั้นพลังงาน จะมีระดับพลังงานชั้นย่อยได้ ไม่เกิน 4 ชั้นย่อย และมีชื่อเรียกชั้นย่อย ดังนี้ s , p , d , f
3. ในแต่ละระดับชั้นพลังงาน จะมีระดับพลังงานชั้นย่อยได้ ไม่เกิน 4 ชั้นย่อย และมีชื่อเรียกชั้นย่อย ดังนี้ s , p , d , f
ในแต่ละชั้นย่อย จะมีจำนวน e - ได้ ไม่เกิน ดังนี้
ระดับพลังงานชั้นย่อย s มี e - ได้ ไม่เกิน 2 ตัว ระดับพลังงานชั้นย่อย p มี e - ได้ ไม่เกิน 6 ตัวระดับพลังงานชั้นย่อย d มี e - ได้ ไม่เกิน 10 ตัว ระดับพลังงานชั้นย่อย f มี e - ได้ไม่เกิน 14 ตัว เขียนเป็น s 2 p 6 d 10 f 14
วิธีการจัดเรียงอิเล็กตรอนในอะตอม
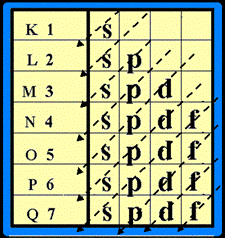
การจัดเรียงอิเล็กตรอน ให้จัดเรียง e- ในระดับพลังงานชั้นย่อยโดยจัดเรียงลำดับตามลูกศร ( แนวทางการจัดเรียงอิเล็กตรอน ให้เขียนแผนผังก่อน ดังรูป
จัดเรียงอิเล็กตรอนตามลูกศร ดังรูป
ตัวอย่าง จงจัดเรียงอิเล็กตรอนของธาตุ คัลเซียม ( Ca )
ธาตุ Ca มีเลขอะตอม = 20 แสดงว่ามี p = 20 และมี e- = 20 ตัว ( ดูเลขอะตอม จากตารางธาตุ)
แล้วจัดเรียง e- ดังนี้
ธาตุ Ca มีเลขอะตอม = 20 แสดงว่ามี p = 20 และมี e- = 20 ตัว ( ดูเลขอะตอม จากตารางธาตุ)
แล้วจัดเรียง e- ดังนี้
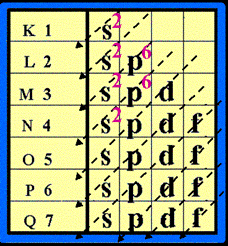
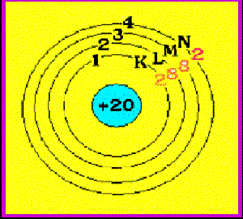
ดังนั้น การจัดเรียง e- ของธาตุ Ca = 2 , 8 , 8 , 2
มีแผนผังการจัดเรียง e- ดังนี้ Ca มีจำนวน e- ในระดับพลังงานชั้นนอกสุด = 2 ตัว จำนวนอิเล็กตรอนในระดับพลังงานชั้นนอกสุด เรียกว่า เวเลนซ์อิเล็กตรอน (Valence electron) ดังนั้น Ca มีเวเลนซ์อิเล็กตรอน = 2 ดังรูป
มีแผนผังการจัดเรียง e- ดังนี้ Ca มีจำนวน e- ในระดับพลังงานชั้นนอกสุด = 2 ตัว จำนวนอิเล็กตรอนในระดับพลังงานชั้นนอกสุด เรียกว่า เวเลนซ์อิเล็กตรอน (Valence electron) ดังนั้น Ca มีเวเลนซ์อิเล็กตรอน = 2 ดังรูป
บทความใหม่กว่า บทความที่เก่ากว่า